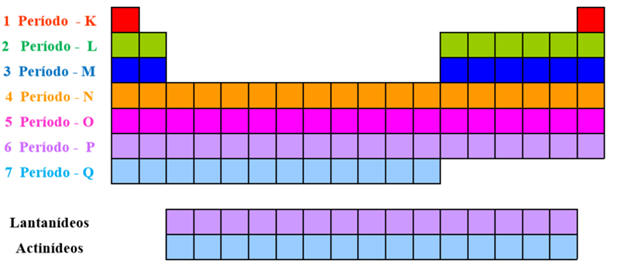
A tabela periódica organiza os elementos em grupos , que são as colunas e períodos , que são as linhas horizontais . O sistema de numeração usada atualmente é recomendado pela União Internacional de Química Pura e Aplicada (IUPAC ). Cada uma das linhas (horizontais) recebe o nome de “Período”. Todos os elementos classificados num mesmo período têm o mesmo número de níveis ou camadas eletrônicas (K = 2, L = 8, M = 18, N = 32, O = 32, P = 18 e Q = 2).
Os períodos são numerados de acordo com o número de níveis eletrônicos de 1 a 7, de cima para baixo. Assim, ohidrogênio (H) e o hélio (He) estão situados no primeiro período, enquanto que o frâncio (Fr) está localizado no sétimo período. À exceção do primeiro, os períodos começam com um metal e terminam com os gases nobres. Os períodos diferem em comprimento, variando de 2 elementos, no primeiro período, o mais curto, a 32 elementos no sexto período, o mais longo.
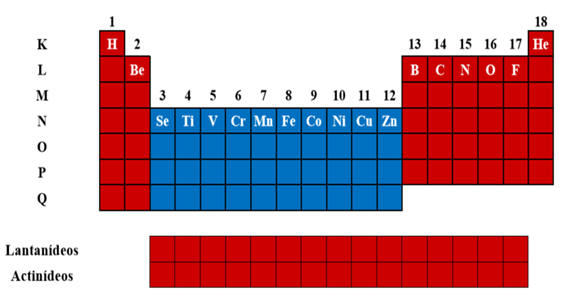
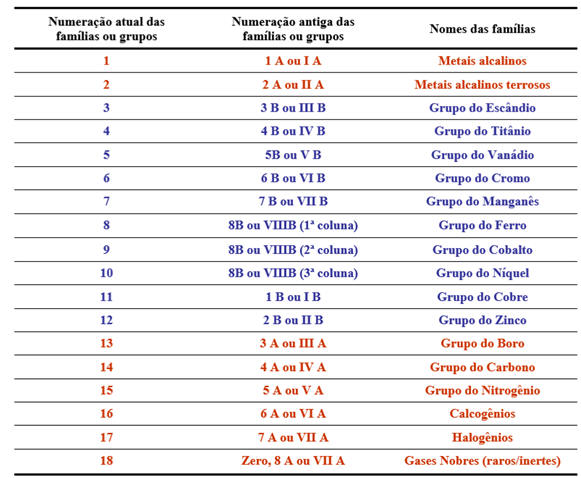
Cada coluna (na vertical) recebe o nome de “Grupo” ou “Família“, e os elementos de uma mesma família apresentam a mesma distribuição eletrônica na camada de valência e propriedades químicas semelhantes. A numeração dos grupos ou famílias é feita em algarismos arábicos de 1 a 18 , crescendo da esquerda para a direita. Apesar disso, ainda é comum usar o sistema de numeração antigo, onde existiam as famílias A e as famílias B.
Representação da coluna Vertical
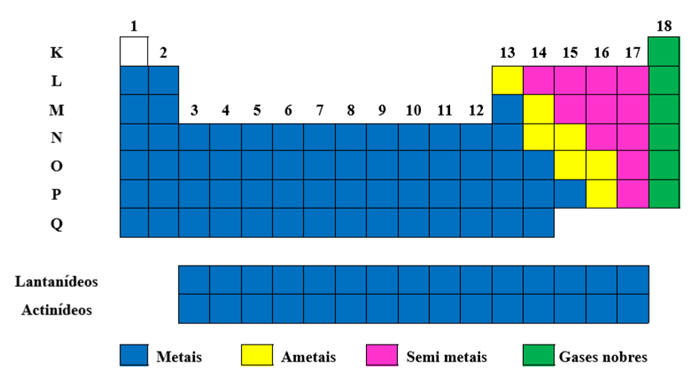
Os elementos podem ser: Metais (possuem todas as propriedades metálicas, como o brilho característico, tipo de ligação, etc.), Não-metais ou Ametais (elementos que não possuem nenhuma semelhança com os metais e, geral, são gasosos), Semi-metais ou Metalóides (elementos que possuem propriedades de metais e de não-metais) e Gases nobres (gases que, por possuírem o último nível de valência completo, não são capazes de estabelecerem ligações químicas com outros elementos, exceto em casos especiais).