ATIVIDADE PRÁTICA: Separação e Identificação dos Pigmentos dos Cloroplastídeos por Cromatografia de Papel
OBJETIVO: Extrair e identificar os pigmentos cloroplastídicos de material vegetal verde.
INTRODUÇÃO
O que se observa no mundo vegetal quanto à coloração típica da parte vegetativa é a predominância da coloração verde, fundamentada pela presença da clorofila. Errôneo seria pensar que nestes vegetais ocorresse apenas a presença dos pigmentos clorofilianos. O que ocorre na realizada é o mascaramento de outros pigmentos, como os carotenóides, pela clorofila ou às vezes da clorofila por outros pigmentos.
Os pigmentos amarelos (carotenóides) são raras vezes visíveis, exceto naquelas folhas em que a clorofila não se desenvolve ou foi destruída devido à senescência ou outras alterações fisiológicas das folhas. As plantas de milho que se desenvolvem no escuro a partir de sementes, por exemplo, não sintetizam clorofila e apresentam geralmente uma coloração amarelada devido a presença de pigmentos amarelos. Parece que todos estes pigmentos existem apenas nos grana dos cloroplastídeos. As clorofilas e os carotenóides são muitas vezes designados pigmentos dos cloroplastídeos.
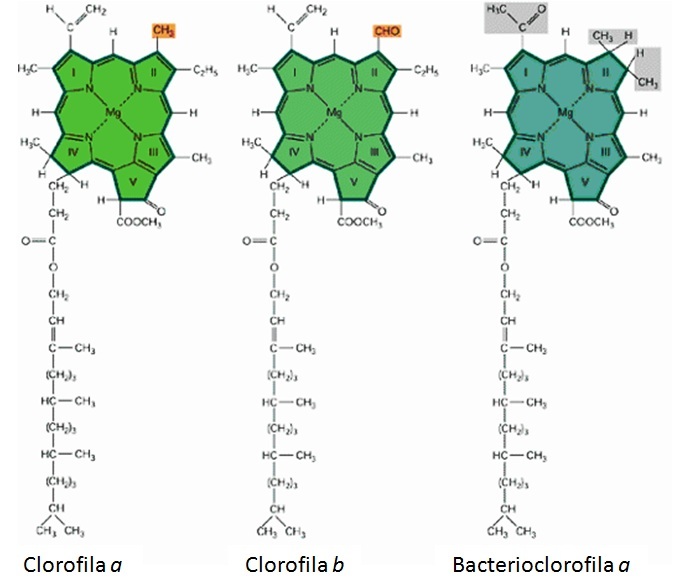
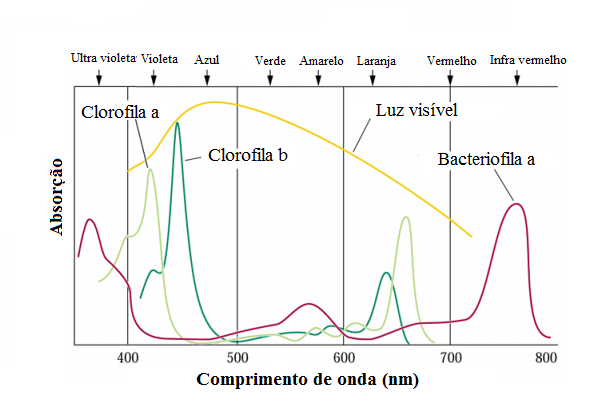
Os compostos químicos mais importantes na conversão da energia luminosa em energia química são os pigmentos que se encontram nos cloroplastos das plantas. É por intermédio deles que a luz inicia o processo da fotossíntese. As clorofilas são os pigmentos fotossínteticos mais importantes das plantas. As clorofilas a e b são as mais conhecidas e as mais abundantes e se encontram em todos os organismos autotróficos, exceto nas bactérias pigmentadas. A diferença entre a clorofila a e b se encontra no átomo C3. A clorofila a tem um grupo metil unido a este carbono e na clorofila b encontra-se um grupo aldeído. Suas proporções são geralmente de 3a:1b. A fórmula molecular da clorofila é C55H-2O5N4MG.
Os carotenóides constituídos exclusivamente por C-H chamam-se CAROTENOS e aqueles que contêm oxigênio são as XANTOFILAS. As xantofilas são mais abundantes na natureza que os carotenos e podem chegar a uma proporção de 2:1. As principais xantofilas encontradas nas folhas verdes são: LUTEÍNA (a CAROTENO), VIOLANXANTINA, ZEAXANTINA (b caroteno).
A clorofila e os carotenóides podem ser separados por cromatografia de papel. A cromatografia baseia-se numa série de fenômenos e métodos físicos usados na química e biologia para separação de componentes de uma mistura. A migração diferencial é o fundamento da cromatografia. A capacidade de migração de cada componente da mistura pode ser determinada pelo seu Rf que é a relação entre a distância percorrida pela substância e aquela percorrida pelo solvente (eluente).
Além das clorofilas e carotenóides, que são lipossolúveis, as plantas possuem outros pigmentos, que são hidrossolúveis (solúveis em água). Os flavonóides, sendo as antocianinas os mais conhecidos, encontram-se dissolvidos no suco celular, no interior do vacúolo, tanto de raízes, como de flores e frutos, conferindo a estes suas cores características. O acúmulo de antocianinas é estimulado por altos níveis de luz, por deficiência de certos nutrientes como N, P, S, etc, e por baixas temperaturas.
METODOLOGIA
- Extração e separação dos pigmentos dos cloroplastídeos em álcool etílico.
Tome alguns pedaços de folhas verdes e coloque-as em um pouco de álcool etílico fervente (banho-maria) até que ocorra a despigmentação.
Coloque a solução de pigmentos num bequer até uma altura de 1cm.
Introduza uma tira de papel de filtro (3 x 15 cm) na solução deixando-a que atinja aproximadamente 4 cm de altura.
Transfira a tira de papel para um bequer contendo 1 cm de altura de álcool etílico e aguarde a separação.
- Extração em acetona e separação em tetracloreto de carbono.
- Tome cerca de 1g de folhas verdes, desprovidas de nervuras maiores.
- Pique as folhas com uma tesoura e junte os pedaços com um pouco de areia num almofariz. Coloque um pouco de acetona (5 a 6 ml) e homogeinize até a obtenção de polpa extremamente fina.
- Filtre o homogenato em algodão num funil de vidro e apare-o num filtro em tubo de ensaio.
- Corte uma tira de papel de filtro de aproximadamente 20 por 4 cm. tomando cuidado de manuseá-lo o mínimo possível (a gordura da mão atrapalha). Trace uma linha de lapis a uma distância de 2 cm da borda de menor dimensão.
- Sature uma câmara cromatográfica (frasco de 500 ml, de boca larga de tampa de rosca ou proveta de 2 l com vedação superior) derramando tetracloreto de carbono (CCL4) até uma altura de 1 cm.
- Com o auxílio de uma micropipeta, tubo capilar, pincel bem fino ou pipeta Pasteur, trace uma linha (tão fina quanto possível) do extrato sobre a marca de lápis. Faça aplicação até que a linha adquira uma coloração verde escura.
- Afixe a tira de papel de filtro numa placa de petri e introduza-a no interior da cubeta até que a extremidade fique submersa 1 cm no solvente.
- Após 60 a 90 minutos identificar os pigmentos, sabendo que a clorofila a é azul-esverdeada, a clorofila b é verde, o caroteno laranja e a xantofila amarela.
QUESTIONÁRIO
- Qual a diferença estrutural entre a clorofila a e a clorofila b?
- Qual a diferença na composição química molecular entre carotenos e xantofilas?
- O que é Rf? Qual é a sua utilidade?
- Qual o grupo de pigmentos mais abundantes na natureza? Qual a proporção entre eles? Cite 3 xantofilas mais abundantes na natureza.
- Faça um cromatograma mostrando os componentes da mistura de pigmentos.
- Que relação existe entre os sintomas de deficiência de Nitrogênio e Magnésio com conteúdo de clorofila?
- Onde se localizam, na célula, as clorofilas, carotenóides e antocianinas?
- Por que podemos afirmar com certeza que as antocianinas não participam da fotossíntese?
- Como se pode explicar a separação pela cromatografia de papel, com base nas estruturas moleculares de cada composto?
- Que diferença foi observada quando do uso de álcool etílico, e tetracloreto de carbo
FIGURA 1. Estrutura de moléculas de clorofilas a e b de plantas (R = CHO, clorofila b;R = CH3, clorofila a) e de uma bacterioclorofila a
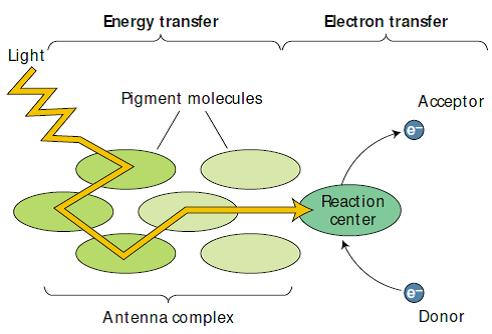
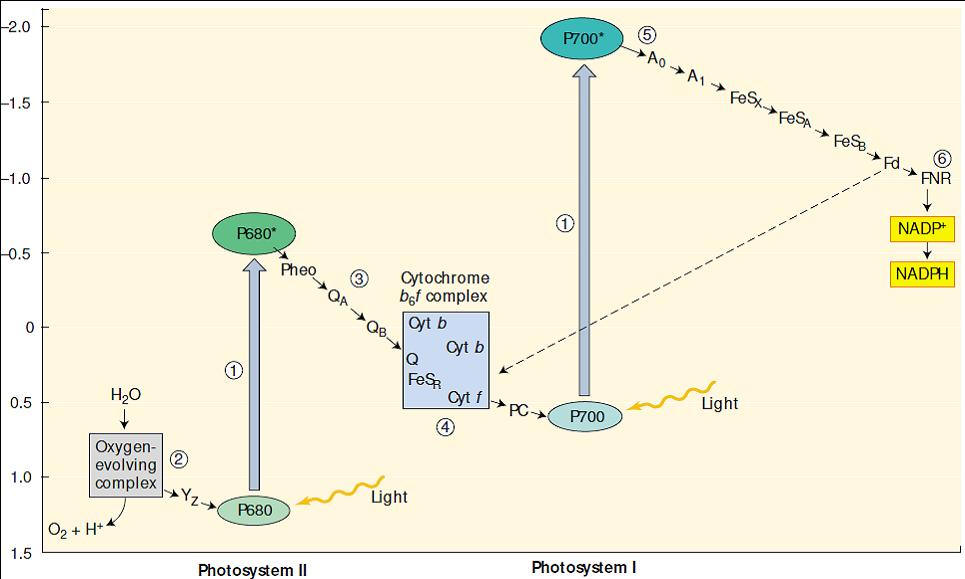
Figura 2. Fotossitema I e II; centro de reação e pigmentos.