Metabolismo celular sob deficiência de oxigênio
Durante o ciclo natural de vida das plantas, é comum que elas passem por períodos de deficiência de oxigênio em suas raízes que, dependendo do tempo e da intensidade, podem levá-las a morte. Excesso de chuvas ou irrigação e solos mal drenados ou compactados são as causas mais freqüentes que influenciam na redução de oxigênio do solo. Nessas condições, a água ocupa os espaços antes preenchidos pelo ar, provocando uma série de mudanças nas características físicas, químicas e biológicas. A difusão do oxigênio na água é 10.000 vezes mais lenta que no ar, tornando o ambiente radicular hipóxico. Além disso, o consumo do oxigênio remanescente devido à respiração dos órgãos submersos da planta e dos microrganismos torna esse ambiente anóxico.
Três tipos de condições são distinguidas baseadas no nível de O2 do ambiente:
A) Normoxia: condições onde a respiração anaeróbica e o metabolismo procedem normalmente e a maioria do ATP é regenerado via fosforilação oxidativa;
B) Hipoxia: condições onde a redução na disponibilidade de O2 começa a se tornar um fator limitante para a produção de ATP através da fosforilação oxidativa;
C) Anoxia: condição em que o ATP produzido é proveniente somente da glicólise, ocorre quando o oxigênio não está mais disponível.
Em qualquer uma dessas situações, o desenvolvimento das plantas é prejudicado. Como conseqüência da falta de oxigênio ocorre uma série de distúrbios no metabolismo das plantas que se manifestam por meio de alterações no crescimento e no desenvolvimento. Essas alterações parecem estar relacionadas aos mecanismos de tolerância, levando a um ajustamento metabólico, anatômico e ou morfológico, que permitem às plantas sobreviverem por períodos mais prolongados nessas condições.
As alterações se manifestam como adaptações morfológicas através da formação de aerênquimas e raízes adventícias, bem como a elongação de caules e folhas. Dentre as alterações metabólicas ou moleculares, devido à baixa disponibilidade de oxigênio, inclui-se o desvio do metabolismo aeróbico para a via anaeróbica, a qual possui baixo rendimento energético. Ao mesmo tempo, ocorre repressão da síntese de polipeptídios aeróbicos e a indução da síntese de polipeptídios anaeróbicos. A maioria desses polipeptídios foi identificada como enzimas envolvidas na fermentação e metabolismo de açúcares-fosfato, cuja síntese é regulada nas etapas transcricionais e pós-transcricionais.
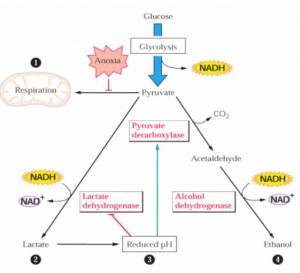
Em condições de ausência de oxigênio, a fermentação regenera o NAD+, que é necessário para dar continuidade à glicólise. Isso porque, nesta condição, o ciclo de Krebs e a cadeia de transporte de elétrons não conseguem funcionar. A glicólise, deste modo, não pode continuar operando, devido ao suprimento da célula em NAD+ ser limitado, e o NAD+ se apresentar disponível em grande maioria no estado reduzido (NADH), a reação catalisada pelo gliceraldeído 3P desidrogenase não pode ocorrer. Para superar este problema, plantas e outros organismos podem metabolizar todo o piruvato através do metabolismo fermentativo (Fig. 1).
Figura 1. Visão geral do metabolismo anaeróbico
Na fermentação alcoólica, as duas enzimas descarboxilase do piruvato e desidrogenase do álcool agem sobre o piruvato, produzindo etanol e CO2 e oxidando NADH no processo. A desidrogenase do álcool e a desidrogenase do lactato são essenciais para operar o ciclo glicolítico sobre condições anaeróbicas, porque elas reciclam NAD+, reduzindo piruvato a etanol e lactato, respectivamente. Esse processo de acúmulo de etanol e lactato envolve a oxidação do NADH e resulta em pequena mas essencial produção de ATP para a sobrevivência de algumas espécies durante a ausência de oxigênio.
Durante as primeiras horas da germinação, as sementes são impermeáveis ao oxigênio, logo, as mesmas rapidamente geram um aumento no coeficiente respiratório, aumenta a atividade da desidrogenase do álcool e ativa a fermentação alcoólica.
Algumas plantas regulam o pH para prevenir a acidificação do citoplasma. A taxa de síntese de lactato e etanol depende do pH citoplasmático. Sobre condições anaeróbicas, o piruvato é inicialmente convertido a lactato, mas como o pH decresce, a atividade da desidrogenase do lactato é inibida, sendo a atividade da descarboxilase do piruvato estimulada, e a síntese do etanol predomina. Apesar da fermentação láctica preceder, a fermentação alcoólica, o acúmulo de lactato acidifica o citosol funcionando como um sinal para a ativação da fermentação alcoólica. O citoplasma acidificado pode estimular a atividade da descarboxilase do piruvato e reduzir a atividade da desidrogenase do lactato. O etanol é o principal produto final do metabolismo anaeróbico em plantas, uma vez que, ao contrário do lactato, não é tóxico e não acidifica o citoplasma.
Fermentação lática
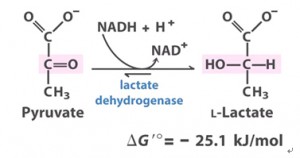
A desidrogenase do lactato (LDH) converte o piruvato a lactato usando NADH como poder redutor e é anaerobicamente induzida em muitas espécies (Fig. 2). A fermentação láctica frequentemente ocorre na germinação das sementes. A atividade da LDH continua a fermentação láctica, mantendo o balanço redox sem a perda do carbono associado com a fermentação alcoólica. A fermentação lática precede a fermentação alcoólica. O lactato pode acidificar o citosol comprometendo a célula. As reações que envolve essa enzima é dependente do pH, o equilíbrio da reação à pH 7,0 fica deslocado para a direita, e pode reverter a reação operando em pH de 8 a 9.
Figura 2. Visão geral da fermentação láctica
Fermentação alcóolica
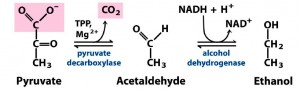
A enzima descarboxilase do piruvato catalisa a descarboxilação do piruvato a acetaldeído (precursor do etanol) e CO2 por meio de uma reação irreversível, necessitando de pirofosfato de tiamina e Mg2+ como cofatores. A reação é marcadamente exergônica, o que significa que os produtos finais da fermentação alcoólica, C2H5OH e CO2 não podem ser convertidos em piruvato novamente. É a primeira enzima na via da fermentação alcoólica e ocupa posição chave no início das rotas metabólicas em anaerobiose. Na reação final da fermentação alcoólica, o acetaldeído é reduzido a etanol pelo NADH na presença da desidrogenase do álcool. Essa reação favorece muito a redução do acetaldeído a pH 7,0. Outra vez, sendo uma reação que envolve uma coenzima nucleotídeo-nicotinaminda, o processo é altamente dependente do pH, e pode-se converter álcool a acetaldeído quantitivamente, isto é, reverter a reação a pH 9,5 em presença de um excesso de NAD+. O NAD+ entra novamente no processo glicolítico (Fig. 3).
Figura 3. Visão geral da fermentação alcoólica
Nos vegetais ocorre principalmente a fermentação alcoólica, a fermentação láctica precedendo a fermentação alcoólica acumula ácido láctico acidificando o citosol e funcionando como um sinal para ativação da fermentação alcoólica. Com o citosol acidificado há um estimulo da atividade da enzima descarboxilase e reduz a atividade da desidrogenase do lactato.
A fermentação de açúcares tem uma função crucial na sobrevivência de plantas à anoxia e a expressão de genes envolvidos nessa rota tem sido extensivamente estudada em níveis de mRNA e proteínas. A desidrogenase alcoólica (ADH), que catalisa a redução do acetaldeído tóxico a etanol, é trancricionalmente induzida em hipoxia ou anoxia. Em raízes de milho, foi observado um aumento de 50 vezes no mRNA dessa enzima, após 5 a 8 horas de hipoxia. Mutantes de Arabidopsis que não expressam a ADH são mais sensíveis ao estresse hipóxico que o tipo selvagem.
A aclimatação à falta de oxigênio não requer somente um rápido aumento nos níveis de enzimas da rota fermentativa, uma vez que a tolerância está relacionada à habilidade de sustentar a fermentação sob períodos prolongados de anoxia. Além disso, a indução de genes no início da adaptação anaeróbica é significativamente diferenciada daquela das fases posteriores. A indução de proteínas sintetizadas durante a aclimatação compreende somente uma pequena porcentagem da síntese total de proteínas e não há referência para inferir que esse pequeno componente contribui exclusivamente para a tolerância à anoxia. Além disso, outras atividades celulares têm sido implicadas na tolerância à baixa concentração de oxigênio, incluindo regulação do pH, sinal de tradução e resistência ao estresse oxidativo pós-anóxico.
Veja mais: Adaptações fisiológicas sob condições de hipoxia ou anoxia
Referências bibliográficas:
Nelson, D. L.; Cox, M. M. Lehninger Princípios de Bioquimíca. 2008
Buchanan, Gruissem, Jones, Biochemistry & Molecular Biology of Plants p. 696-705. 2000
Taiz, L.; Zeiger, E. Fisiologia vegetal. 5. ed. Porto Alegre: Artmed, 2012. 820 p.
Artigos:
http://www.annualreviews.org/doi/pdf/10.1146/annurev.arplant.59.032607.092752
http://ledson.ufla.br/MPS/SITES/Respira%C3%A7%C3%A3o/MetabolismoAnaerobico/Artigo2.pdf