As plantas requerem certo número de elementos além daqueles que obtém diretamente da atmosfera (carbono e oxigênio sob a forma de dióxido de carbono) e da água do solo (hidrogênio e oxigênio). Todos estes elementos, com exceção de um, provêm da desintegração das rochas e são captados pelas plantas a partir do solo. A exceção é o nitrogênio, que representa 78% da atmosfera terrestre. Embora as rochas da superfície terrestre constituam também a fonte primária de nitrogênio, este penetra no solo, indiretamente por meio da atmosfera, e, através do solo, penetra nas plantas que crescem sobre ele. Entretanto, a maioria dos seres vivos é capaz de utilizar o nitrogênio atmosférico para sintetizar proteínas e outras substâncias orgânicas. (Ao contrário do carbono e do oxigênio, o nitrogênio é muito pouco reativo do ponto de vista químico, e apenas certas bactérias e algas azuis possuem a capacidade altamente especializada de assimilar o nitrogênio da atmosfera e convertê-lo numa forma que pode ser usada pelas células. A deficiência de nitrogênio utilizável constitui muitas vezes, o principal fator limitante do crescimento vegetal.
ASSIMILAÇÃO E TRANSPORTE DE NITROGÊNIO NA PLANTA
Em plantas superiores a assimilação de nitrogênio (N) é o segundo maior processo metabólico, sendo superado apenas pela fixação fotossintética do CO2.Com isto, o nitrogênio (N) é o mineral que se apresenta em maiores níveis nos vegetais superiores. As principais formas de N no solo, disponíveis às plantas, são a nítrica e a amoniacal, embora a quantidade de N disponível no solo normalmente é pequena quando comparada com a quantidade total, ou seja, próximo a 5% ou menos. O restante do N se encontra em combinações orgânicas que não são prontamente aproveitáveis pelos vegetais.
A nutrição nitrogenada dos vegetais fica na dependência da transformação do N-orgânico para as formas minerais aproveitáveis, através do processo de mineralização, mediado por microorganismos, formando amônio e nitrato, que são formas prontamente disponíveis para a planta. Sendo que, o nitrato é a principal forma de N mineral nos solos cultivados (Clarke e Barley, 1968), visto que o N-NH4+ proveniente da decomposição da matéria orgânica ou adicionado ao solo como fertilizante é gradativamente convertido a N-NO3– naqueles solos.Diversos estudos têm demonstrado que o emprego de N-amoniacal como única forma de N é prejudicial para o crescimento de algumas espécies vegetais . Porém, a adição de nitrato ameniza os efeitos inibitórios do amônio sobre o crescimento .
O processo de absorção do nitrato difere dos demais nutrientes pelo fato da absorção nítrica ser induzida pelo próprio íon . Embora a absorção de nitrato e amônio seja mediada por transportadores, a absorção nítrica ocorre contra um gradiente de potencial eletroquímico, ao passo que a absorção amoniacal é menos dependente de energia . Lemos, Delú e Oliveira (1999), constataram que a assimilação do N, em plantas jovens de seringueira, ocorre basicamente em raízes. Tal fato indica que, nos tecidos radiculares de plantas de seringueira, há uma demanda significativa de carbono fixado para a biossíntese de compostos nitrogenados.
Muitos estudos têm sido realizados sobre o papel do sistema aéreo, em particular os cloroplaastos, no metabolismo do nitrogênio em plantas superiores. Na maioria das espécies estudadas as folhas são os principais sítios de redução do nitato e das conseqüentes reações de assimilação do amônio e biossíntese de aminoácidos. No entanto, essas generalizações feitas foram baseadas em espécies herbáceas de ciclo curto. Tem sido sugerido que em espécies perenes de clima temperado a assimilação do nitrogênio se dá predominantemente na raiz, enquanto que em espécies perenes de clima tropical isto ocorre principalmente nas folhas.
A maioria das espécies cultivadas utilizam o nitrato como fonte de nitrogênio e seu efeito no metabolismo geral da planta tem sido muito estudado. Após sua absorção, o nitrato é reduzido para amônio, o qual é depois assimilado a aminoácidos. A redução do nitrato ocorre em dois estágios, com o nitrato sendo o produto intermediário na presença de duas enzimas a Redutase do Nitrato (RN) e a Redutase do Nitrito (RNi).
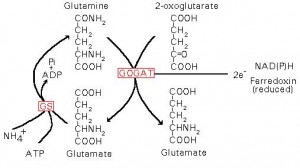
Glutamina e glutamato são considerados os produtos primários da assimilação do amônio, com as enzimas Glutamina Sintetase (GS) e Glutamato Sintetase (GOGAT) atuando como catalizadores do ciclo do glutamato, no qual o glutamato é tanto substrato como produto final. A redução e assimilação podem ocorrer nas raízes ou folhas sendo que as proporções relativas variam entre estes dois sítios com a espécie e condições ambientais.
A ação conjunta da GS/GOGAT tem sido denominada ciclo do glutamato. Neste ciclo a GS produz grandes quantidades de glutamina, a qual exige igual quantidade de a-cetoglutarato proveniente da respiração mitocondrial de fotossintatos, como esqueletos de carbono necessários para formar glutamato.
Figura 1: Sistema GS/GOGAT de assimilação do amônio (Lee et al., 1992).
A enzima sintase do glutamato (conhecida como glutamina 2-oxoglutarato aminotransferase, ou GOGAT) catalisa a conversão de glutamina e 2-oxoglutarato em duas moléculas de glutamato. Duas diferentes formas da enzima estão presentes em plantas superiores, sendo que uma utiliza NADH como fonte de poder redutor e, a outra, a ferrodoxina. A enzima dependente de ferrodoxina é uma proteína monomérica com peso molecular de 140-160 KDa. Ela está localizada nos cloroplastos de folhas e sua atividade aumenta durante o desenvolvimento das folhas, sob condições de luz e está envolvida no metabolismo fotorrespiratório do nitrogênio. A atividade da enzima dependente de NADH tem sido detectada em tecidos não verdes, a exemplo de raízes e feixes vasculares. É um monômero de peso molecular entre 200-225 KDa. Nas raízes, a NADH-GOGAT está envolvida na aasimilação do NH4+ absorvido na rizosfera. Enquanto que, nos feixes vasculares de folhas em desenvolvimento, a NADH-GOGAT assimila a glutamina translocada das raízes ou das folhas senescentes. Detalhes das reações catalisadas pelas enzimas GS e GOGAT podem ser vistos na figura abaixo:
O amônio pode ser assimilado através de uma rota alternativa, conhecida como rota da glutamato desidrogenase (GDH). A enzima glutamato desidrogenase catalisa a reação reversível que sintetiza ou desamina o glutamato. Uma forma NADH-dependente da GDH é encontrada nas mitocôndrias e uma forma NADPH-dependente ocorre nos cloroplastos de órgãos fotossintetizantes. Embora ambas as formas sejam relativamente abundantes, elas não podem substituir a rota da GS/GOGAT para assimilação do amônio, tendo como função principal desaminar o glutamato.
As leguminosas fixadoras de nitrogênio podem ser divididas em exportadoras de amidas ou exportadoras de ureídeos, com base na composição da seiva do xilema. As amidas, principalmente os aminoácidos ASPARAGINA E GLUTAMINA , são exportadas por leguminosas de regiões temperadas, tais como ervilha, trevo, fava e lentilha. Os ureídeos são exportados por leguminosas de origem tropical, tais como a soja, o feijão, o amendoim e a Vigna. Os três ureídeos principais são a alantoína, ácido alantóico e citrulina. A alantoína é sintetizada nos peroxissomos a partir do ácido úrico, enquanto o ácido alantóico é sintetizado a partir da alantoína no retículo endoplasmático. O local de síntese da citrulina a partir do aminoácido ornitina ainda não foi determinado. Os três compostos são liberados no xilema e transportados para a parte aérea, onde são rapidamente catabolizados a amônio.
A alantoina é sintetizada nos peroxissomos a partir do ácido úrico, enquanto o ácido alantóico é sintetizado a partir da alantoína no retículo endoplasmático. O local de síntese da citrulina, a partir do aminoácido ornitina, ainda não foi determinado. Os três compostos são liberados no xilema e transportados para a parte aérea, onde são rapidamente catabolizados a amônio. Esse amônio entra na rota de assimilação já descrita. As plantas não nodulares por sua vez, a forma preferencial de transporte de nitrogênio depende, em grande, parte das condições ambientais. Em condições de alta concentração de NO3– este pode ser transportado para posterior redução nas folhas em um grande número de espécies vegetais. Entretanto, a principal forma de transporte de nitrogênio nesses vegetais é na forma amídica.
PERDA DE NITROGÊNIO
Conforme observamos os compostos nitrogenados das plantas clorofiladas retornam ao solo com a morte das mesmas (ou dos animais que delas se alimentaram), sendo reprocessados pelos organismos e microrganismos do solo, absorvidos pelas raízes sob a forma de nitrato dissolvido na água do solo e reconvertidos em compostos orgânicos. Durante o decorrer deste ciclo verifica-se sempre uma “perda” de certa quantidade de nitrogênio, no sentido de se tornar inutilizável para a planta. Uma das principais causas desta perda de nitrogênio é a remoção de plantas do solo. Os solos cultivados exibem freqüentemente um declínio constante no conteúdo de nitrogênio. O nitrogênio pode ser também perdido quando a parte superficial do solo é decapitada pela erosão ou quando sua superfície é destruída pelo fogo. O nitrogênio é também removido pela lixiviação; os nitratos e nitritos, que são anions, mostram-se particularmente suscetíveis à lixiviação pela água que se infiltra através do solo. Em alguns solos, bactérias desnitrificantes decompõem os nitratos e liberam nitrogênio para o ar. Este processo que fornece à bactéria o oxigênio necessário para a respiração é dispendioso em termos de necessidades energéticas (isto é, o O2 pode ser reduzido mais rapidamente que o NO3–) e ocorre extensamente apenas nos solos com deficiência de oxigênio, isto é, nos solos que são mal drenados e, portanto, pobremente arejados.
Algumas vezes uma alta proporção do nitrogênio presente no solo não é disponível para as plantas. Esta imobilização ocorre quando existe excesso de carbono. Quando substâncias orgânicas ricas em carbono, mas pobres em nitrogênio, a palha é um bom exemplo, se encontram em abundância no solo, os microrganismos que atacam estas substâncias precisarão de mais nitrogênio do que contêm a fim de utilizar totalmente o carbono presente. Em conseqüência, não utilizarão apenas o nitrogênio presente na palha ou material semelhante, mas também todos os sais de nitrogênio disponíveis no solo. Conseqüentemente, este desequilíbrio tende a normalizar-se à medida que o carbono é fornecido sob a forma de dióxido de carbono pela respiração microbiana, e à medida que aumenta a proporção entre nitrogênio e carbono no solo.
FIXAÇÃO DE NITROGÊNIO
A fixação do nitrogênio é o processo pelo qual o nitrogênio gasoso do ar é incorporado em compostos orgânicos nitrogenados e, assim, introduzido no ciclo do nitrogênio. A fixação deste gás, que pode ser efetuada, em graus apreciáveis, por apenas algumas bactérias e algas azuis, é um processo do qual dependem atualmente todos os organismos vivos, da mesma forma que todos eles dependem, em última análise, da fotossíntese para a obtenção de energia.
Uma a duas centenas de milhões de toneladas métricas de nitrogênio são acrescentadas à superfície terrestre a cada ano pelos sistemas biológicos. O homem produz 28 milhões de toneladas métricas, cuja maior parte é utilizada como fertilizantes; no entanto, este processo é efetuado com alto custo energético em termos de combustíveis fôsseis. A quantidade total de energia necessária para a produção de fertilizantes de amônio é atualmente estimada como equivalente a 2 milhões de barris de óleo por dia. De fato, calcula-se que os custos da fertilização com nitrogênio estão atingindo o ponto de lucros decrescentes. As culturas tradicionais em áreas tais como a Índia não atingem uma produção significativamente aumentada com a utilização de fertilizantes com nitrogênio, tendo baixas necessidades deste elemento, mas estão sendo atualmente substituídas por “cereais milagrosos” e outras culturas que não produzem mais com fertilização com nitrogênio – justamente numa época em que tal tratamento está se tornando proibitivamente dispendioso.
Das várias classes de organismos fixadores de nitrogênio, as bactérias simbióticas são, incomparavelmente, as mais importantes em termos de quantidades totais de nitrogênio fixado. A mais comum das bactérias fixadoras de nitrogênio é Rhizobium, que é um tipo de bactéria que invade as raízes de leguminosas (angiospermas da família Fabaceae ou Leguminosae), tais como trevo, ervilha, feijão, ervilhaca e alfafa.
Os efeitos benéficos das leguminosas sobre o solo são tão óbvios que foram reconhecidos há centenas de anos. Teofrasto, que viveu no terceiro século a.C. escreveu que os gregos utilizavam culturas de feijão para enriquecer os solos. Nos locais em que as leguminosas crescem, certa quantidade de nitrogênio “extra” pode ser liberada para o solo, onde se torna disponível para outras plantas. Na agricultura moderna constitui prática comum alternar uma cultura não leguminosa, como o milho, com uma leguminosa, como a alfafa. As leguminosas são então colhidas para feno deixando as raízes ricas em nitrogênio, ou ainda melhor, são aradas novamente no campo. Uma boa colheita de alfafa, que é recolocada no solo, pode fornecer 450 quilogramas de nitrogênio por hectare. A aplicação dos elementos vestigiais, cobalto e molibdênio, exigidos pelas bactérias simbióticas, incrementa grandemente a produção de nitrogênio se estes elementos estiverem presentes em quantidades limitantes, como em grande parte da Austrália.
AMONIFICAÇÃO
Grande parte do nitrogênio encontrado no solo provém de materiais orgânicos mortos, nos quais existe sob a forma de compostos orgânicos complexos, tais como proteínas, aminoácidos, ácidos nucleicos e nucleótides. Entretanto, estes compostos nitrogenados são, em geral, rapidamente decompostos em substâncias mais simples por organismos que vivem nos solos. As bactérias saprófitas e várias espécies de fungos são os principais responsáveis pela decomposição de materiais orgânicos mortos. Estes microrganismos utilizam as proteínas e os aminoácidos como fonte para suas próprias proteínas e liberam o excesso de nitrogênio sob a forma de amônio (NH4+ ). Este processo é denominado amonificação. O nitrogênio pode ser fornecido sob a forma de gás amoníaco (NH3), mas este processo ocorre geralmente apenas durante a decomposição de grandes quantidades de materiais ricos em nitrogênio, como numa grande porção de adubo ou fertilizante. Em geral, a amônia produzida por amonificação é dissolvida na água do solo, onde se combina a prótons para formar o íon amônio.
NITRIFICAÇÃO
Várias espécies de bactérias comumente encontradas nos solos são capazes de oxidar a amônia ou amônio. A oxidação do amoníaco, conhecida como nitrificação, é um processo que produz energia e a energia liberada é utilizada por estas bactérias para reduzir o dióxido de carbono, da mesma forma que as plantas autotróficas utilizam a energia luminosa para a redução do dióxido de carbono. Tais organismos são conhecidos como autotróficos quimiossintéticos (diferentes dos autotróficos fotossintéticos, como as plantas e as algas). As bactérias nitrificantes quimiossintéticas Nitrosomonas e Nitrosococcus oxidam o amoníaco dando nitrito (NO2–):
2 NH3 + 3O2 → 2 NO2– + 2 H+ + 2 H2O
O nitrito é tóxico para as plantas superiores, mas raramente se acumula no solo. Nitrobacter, outro gênero de bactéria, oxida o nitrito, formando nitrato (NO3–), novamente com liberação de energia:
2 NO2– + O2 → 2 NO3–
O nitrato é a forma sob a qual quase todo o nitrogênio se move do solo para o interior das raízes. Poucas espécies vegetais são capazes de utilizar proteínas animais como fonte de nitrogênio. Estas espécies, que compreendem as plantas carnívoras, possuem adaptações especiais utilizadas para atrair e capturar pequenos animais. Digerem-se, absorvendo os compostos nitrogenados e outros compostos orgânicos e minerais, tais como potássio e fosfato. As plantas carnívoras em sua maioria são encontradas em pântanos, que são em geral fortemente ácidos e, portanto, desfavoráveis ao crescimento de bactérias nitrificantes
MICROORGANISMOS FIXADORES DE NITROGÊNIO
As bactérias não simbióticas dos gêneros Azotobacter e Clostridium são capazes de fixar o nitrogênio. Azotobacter é aeróbico, ao passo que Clostridium é anaeróbico; ambas são bactérias saprófitas comuns encontradas no solo. Calcula-se que elas fornecem provavelmente cerca de 7 quilogramas de nitrogênio por hectare de solo por ano. Outro grupo importante inclui muitas bactérias fotossintéticas. As algas azuis de vida livre desempenham também um papel importante na fixação do nitrogênio. São cruciais para o cultivo do arroz, que constitui a principal dieta de mais da metade da população mundial. As algas azuis podem desempenhar também um importante papel ecológico na fixação do nitrogênio nos oceanos.
A distinção entre fixação do nitrogênio por organismos de vida livre e simbióticos pode não ser tão rigorosa como se pensava tradicionalmente. Alguns micróbios ocorrem regularmente no solo, ao redor das raízes de certas plantas que eliminam carboidratos, consumindo estes compostos e, ao mesmo tempo, fornecendo indiretamente nitrogênio para as plantas. As associações simbióticas entre bactérias normalmente de vida livre, como Azotobacter, e as células de plantas superiores em culturas de tecido induziram seu crescimento num meio artificial carente de nitrogênio.
ASSIMILAÇÃO DE ENXOFRE
O enxofre está entre os elementos mais versáteis dos organismos vivos. As pontes dissulfídicas em proteínas exercem funções estruturais e reguladoras. O enxofre participa no transporte de elétrons por meio de grupos ferro-enxofre. Os sítios catalíticos de várias enzimas e coenzimas, tais como uréase e coenzima A, contém enxofre. A versatilidade do enxofre deriva, em parte, da propriedade que apresentam em comum com o nitrogênio: múltiplos estados estáveis de oxidação. O sulfato é a forma de absorção do enxofre nos vegetais.
A maioria do enxofre nas células dos vegetais superiores deriva do sulfato absorvido via um transportador do tipo simporte. O sulfato do solo é proveniente do desgaste das rochas. Entretanto, a queima de combustíveis fósseis libera várias formas de enxofre gasoso, incluindo dióxido de enxofre e sulfeto de hidrogênio, os quais são levados para o solo pela água da chuva.As plantas também podem metabolizar o dióxido de enxofre, que é absorvido na forma gasosa, através dos estômatos.Quando dissolvido em água, o dióxido de enxofre é hidrolisado e transforma-se em ácido sulfúrico.A maior parte do enxofre orgânico está presente no aminoácidos Cisteína e Metionina.
A assimilação do sulfato necessita da redução do sulfato a cisteína:
1 –A primeira etapa da assimilação, é a redução do sulfato ao aminoácido cisteína. O sulfato é muito estável e precisa ser ativado antes que alguma reação subseqüente possa ocorrer. A ativação inicia-se com a reação entre o sulfato e o ATP, para formar Adenosina- 5- fosfosulfato(APS) e pirofosfato (PiPi). A enzima que catalisa essa reação é o ATPsulfurilase.
2 – A reação da ativação é energeticamente desfavorável. Para levar essa reação adiante, os produtos APS e PiPi devem ser convertidos de imediato em outros compostos. O Ppi é hidrolisado a fosfato inorgânico pela pirofosfatase inorgânica.
3 – O APS é rapidamente reduzido ou sulfatado, sendo predominante a via de redução que ocorre exclusivamente nos plastídeos. De inicio a APS redutase, aparentemente, transfere dois elétrons da Glutationa reduzida(GSH) para produzir Sulfito.
4 -A seguir a sulfito redutase transfere 6 elétrons da Ferredoxina reduzida para produzir Sulfeto.
5 – O Sulfeto resultante reage com o O-Acetilserina(OAS) para formar cisteína e acetato. A OAS que reage com o sulfeto, é formada na reação catalisada pela serina acetiltransferase.
6 – A reação que produz cisteína e acetato, é catalisada pela OAS tioliase.
7 -A sulfatação do APS, localizada no citossol é a via alternativa. Inicialmente, a APSquinase catalisa a reação da APS com ATP, para formar 3-fosfoadenosina 5-fosfosulfato(PAPS). A sulfotransferases, então podem transferir o grupo sulfato do PAPS para vários compostos, incluindo colina, flavonol, ácido gálico glicosídeo, glucosinatos, peptídeos e polissacarídeos.
A assimilação do sulfato ocorre principalmente na folha. A redução do sulfato à cisteína altera o número de oxidação do enxofre de +6 para –4, assim necessitando da transferência de 10 elétrons. A glutationa, a ferredoxina, o NAD(P)H ou a o-acetilserina podem atuar como doadores de elétrons em vários passos da rota metabólica.
Na assimilação do enxofre, as folhas são em geral mais ativas doque as raízes, provavelmente devido ao fato da fotossíntese disponibilIzar a ferredoxina reduzida e a fotorespiração gerar a serina, que pode estimular a produção de o-acetilserina. O enxofre assimilado nas folhas é exportado pelo floema para os locais de síntese protéica( frutos e ápices caulinares e radiculares), sobretudo na forma de glutationa.A glutationa também atua como um sinal que coordena a absorção do sulfato pelas raízes e a assimilação pela parte aérea.
A metionina, um outro aminoácido contendo enxofre, encontrado nas proteínas, é sintetizada nos plastídeos a partir da cisteína. Após as sínteses de cisteína e metionina, o enxofre pode ser incorporado nas proteínas e em diversos outros compostos, tais como, Acetil Coa e o S-Adenosilmetionina, sendo este último muito importante para a síntese do Etileno e em reações envolvendo a transferência de grupos metil, como na síntese de lignina.
ABSORÇÃO, TRANSPORTE E REDISTRIBUIÇÃO DE POTÁSSIO
O K na solução do solo e o trocável representam conjuntamente a reserva imediata do elemento no solo e os métodos de rotina para avaliação da fertilidade extraem ambos. Quando devido à remoção pelas culturas e exportação como produto colhido o K na solução cai a concentrações muito baixas (0,02 a 0,100 milimoles/litro ou 0,78 a 3,9 ppm) o equilíbrio se desloca da direita para a esquerda: o potássio é liberado dos minerais primários mais facilmente intemperizáveis passando para o complexo de troca e desta para a solução. Esses minerais constituem, pois, a reserva de K a longo e médio prazo . LEONARD (1985) ilustra a hipótese de absorção do K com a ajuda de uma proteína carregadora específica localizada na membrana celular. A proteína fornece um canal aquoso que atravessa a camada lipídica do plasmalema. A operação desse mecanismo está de acordo com o modelo de cinética enzimática e explica a competição efetuada por íons semelhantes ao K+ na absorção.
A absorção do K, entretanto se dá também graças à atividade de ATPase da membrana celular que o elemento é capaz de ativar. Não se sabe se a ATPase é o mesmo carregador de potássio ou se funciona como bomba que faz a extrusão de H+ trocado pelo K. Alguns aspectos de absorção do K, mais práticos: eles são na verdade, conseqüência dos fatores que influenciam-na em condições controladas. O transporte a longa distância do K ocorre via floema e xilema e o do elemento absorvido pelas folhas o faz via floema, como acontece com os demais elementos móveis. O K pode ser considerado o mais móvel dos nutrientes no sistema solo-planta-atmosfera e, particularmente, na planta. A movimentação na planta – dentro da raiz, desta para a parte aérea, é permitida ou facilitada pelo fato de que, diferentemente dos outros elementos, o K se encontra nos tecidos em maior proporção na forma iônica. De fato, a proporção dos elementos solúveis em água, como porcentagem do extraído por HCl a 1%, é: Ca – entre 1,8% e 59%; Mg – entre 30% e 81%; K – entre 81% e 97%.
Pode-se admitir que essa solubilidade maior do K permite a sua redistribuição, o que usualmente não acontece com o cálcio (Ca) e, muitas vezes, com o magnésio (Mg). Isto porque o K solúvel atravessaria mais facilmente as membranas (plasmalema e tonoplasto) com movimento nos dois sentidos, entrada ou influxo, isto é, absorção propriamente dita, e saída ou efluxo. A saída do K pode ser conseqüência do desarranjo funcional das membranas. Por exemplo, os grãos de café de má qualidade, avaliada pela prova da xícara ou por outro processo, como a atividade da polifenoloxidase, perdem solutos, principalmente K, quando, verdes e moídos, são colocados em contato com um volume determinado de água.
A condição obrigatória para a absorção de K é o estabelecimento de seu contato com a raiz, o que pode se dar por três processos diferentes:
a. Intercepção radicular – ao se desenvolver, a raiz encontra o K da solução do solo, quer seja natural ou adicionado como adubo;
b. Fluxo de massa – o K caminha no solo em uma fase aquosa móvel, a solução do solo, a favor do gradiente de umidade, isto é, de uma região mais úmida e distante da raiz para outra mais seca e próxima da raiz;
c. Difusão – o K+ se movimenta no solo dentro de uma fase aquosa estacionária, a mesma solução do solo, a favor do gradiente de concentração, ou seja, de uma região de maior concentração para outra de menor concentração na superfície da raiz, obedecendo à primeira lei de Fick:
y = – q D dc/dx sendo:
y = fluxo;
q = espaço de poro/volume de solo (o sinal negativo indica que o
movimento se dá na direção oposta à do gradiente de concentração);
D = coeficiente de difusão (cm2 seg-1);
c = concentração;
x = distância.