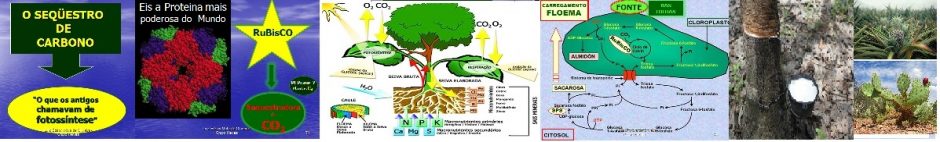
A síntese de sacarose é realizada principalmente pela sacarose fosfato sintase (SPS), uma enzima alostérica ativada pela glucose- 6-fosfato e inibida pelo ortofosfato. A degradação da sacarose, e consequentemente, o estabelecimento do dreno, pode ser realizada tanto pela sacarose sintase (SuSy) quanto pela invertase (Taiz & Zeiger, 2013).
A SuSy apresenta seis isoformas, podendo estar localizadas no citosol, no vacúolo, associada à plasmalema e ao citoesqueleto (Bieniawska et al., 2007; Barrat et al., 2001). Sua principal função é clivar a sacarose para síntese de amido (Déjardin et al., 1997) e parede celular (Nakai et al., 1999), pelo simples fato de que um dos produtos de sua hidrólise é UDP-glicose, precursor para síntese de amido e parede celular. A forma citosólica pode fornecer produtos para o metabolismo geral, enquanto a forma associada à plasmalema pode fornecer UDP-glicose, diretamente para a síntese de celulose e calose (Amor et al., 1995).
Em muitos tecidos-dreno de crescimento e armazenamento ativo, a atividade da SuSy é bastante alta (Ross & Davies, 1992), e a sua atividade pode servir como um indicador bioquímico de crescimento ativo do dreno (Sun et al., 1992; Sung et al., 1989.). Ressalta-se que a atividade da SuSy é geralmente baixa em tecidos-fonte, como em folhas, ocorrendo o oposto em tecidos-dreno (Ress, 1984). A atividade da SuSy está fortemente associada com a bainha vascular, dessa forma, a presença da enzimas nas vertentes ou imediatamente no sistema vascular pode ser um atributo importante deste tecido. A SuSy com sua habilidade de clivar a sacarose pode providenciar substratos necessários para as demandas respiratórias de células ativas do floema além de ter função na síntese de calose, que é comum em plantas superiores. A calose está associada no entupimento de vasos depois de injúrias e no controle da via simplástica através de plasmodesmas. (Wolf et al., 1991).
Dados de estudos mostram previamente que a SuSy tem alta atividade nas áreas vasculares, com específica localização nas células companheiras. Nolte e Koch (1993) avaliaram a presença de SuSy nos tecidos de transporte de milho e trigo. Como resultados eles concluíram que a SuSy do local de carregamento de assimilados e das zonas de transporte estão localizadas principalmente nos tecidos de floema. Entretanto a função fisiológica exata nas células companheiras ainda precisa de muitos estudos, um papel potencial pode estar relacionado com a demanda de energia para o carregamento de sacarose no apoplasto. Investigações fisiológicas e estruturais prévias sugerem que os mecanismos primários para o transporte de solutos nos elementos crivados é susceptível de envolver acumulação ativa do apoplasto nestes sistemas (Humphreys, 1978; Daie, 1989).
As invertases catalisam a hidrólise altamente exotérmica e irreversível da sacarose em glicose e frutose. Em contraste, uma clivagem reversível da sacarose é catalisada pela sintase da sacarose, em UDPG e frutose, possuindo um papel importante no metabolismo da sacarose em diversas rotas bioquímicas relacionadas a funções metabólicas, estruturais e de armazenamento em células de plantas (Winter & Huber, 2000).
Para o descarregamento apoplástico as enzimas invertases são fundamentais. É necessário que se mantenha o potencial de sacarose sempre baixo na célula receptora durante o processo de descarregamento, para que não haja refluxo desse açúcar. Em órgãos com descarregamento simplástico, o baixo potencial químico de sacarose é mantido pela respiração ou pela conversão dos açúcares transportados em compostos necessários para o crescimento ou em polímeros de estoque. Já em órgãos com descarregamento apoplástico, as invertases desempenham um papel central na manutenção de um baixo potencial de sacarose para que haja uma chegada contínua desse composto nas células receptoras (Patrick, 1997).
A enzima invertase pode agir em diversos locais na célula receptora e sua ação é em conjunto com os transportadores de açúcares. Se a atividade da invertase é no apoplasto, a entrada do assimilado na célula receptora requer a presença de transportadores de hexose na plasmalema. Por outro lado, se sua ação é no citoplasma ou no vacúolo, transportadores de sacarose devem estar presentes na plasmalema ou no tonoplasto, respectivamente. As invertases e os carreadores de açúcares também podem funcionar como mecanismos de recuperação de açúcares que se perdem para o apoplasto durante o descarregamento simplástico (Patrick, 1997). Desse modo, espécies com carregamento simplástico podem ter uma via apoplástica paralela. Um exemplo disso parece ser a batata, pois apesar de possuir um descarregamento simplástico, a superexpressão de invertase no apoplasto do tubérculo tende a aumentar a acumulação de matéria seca nesse órgão (Frommer & Sonnewald, 1995). Acredita-se que a invertase ácida da parede celular desempenhe papel importante na assimilação de sacarose fora dos tecidos-dreno, no apoplasto, estabelecendo um gradiente de concentração de sacarose, da fonte para o dreno (Escherich, 1980). A invertase neutra ou alcalina é considerada uma enzima de “manutenção”, envolvida na degradação da sacarose, quando as atividades da invertase ácida e da SuSy são baixas (Winter & Huber, 2000), normalmente em tecidos cuja taxa metabólica é menor, quando comparada à de tecidos meristemáticos, por exemplo (Cunha, 2007).
Referências bibliográficas
BIENIAWSKA Z., BARRAT D.H.T, CARLICJ, THOLEVE V. KRUNGER N.J., MARTIN C.;ZEMNER R. SMITH A.M. Analysus of the sucrose synthese gene family in Arabidopis. The Plant Journal, 2007.
BARRAT D.H.P., BARKER L., KRUGER N. J., SMITH A. M., WANG T.L., MARTINE. Multiple, distinct isoforms of sucrose synthase in pea. Plant Physiology, 655-664. 2001.
DÉJARDIN A., ROCHAT C., WUILLÉM S., BOUTIN J.P. Contribution of sucrose synthase. Plant, Cell and Environment, 1421-1430. 1997.
AMOR Y., HAIGLER C.H.; WAINSCOTT M.; DELMER D.A; Membrane associated formo of SUSy and its potencial role in the synthesis of cellulose and callose in plants. Proceesings of the NAtional Academy of Sciences, 9353-9357. 1995.
NAKAI, T., TONOUCHI N., KONISHI T., TSUCHIDA T., YOSHINAGA F., SAKAI F., HAYASHI T., Enhancement of cellulose production by expression of sucrose snthase in Acetobacter xylinum, Proceedings of the National Academy of Sciences. p. 14-18,1999.
ROSS H. A., DAVIES H.V. Sucrose metabolism in tuber of potato (Solanun tuberosum L.) Efefects of sink removal and sucrose flux on sucrose degrading enzymes. Plant Physiology,p. 287-293.1992.
SUN J.D., LOBODA T., Sung S.J.S, BLACK Jr. C.C . Sucrose synthase in wild tomato, Lycopersicon chmielewskii, and tomato fruit sink strength. Plant Physiology, p. 1163-1169. 1992.
SUNG S.S., XU D.P., Black C.C. Identification of actively filing sucrose sinks. Plant Physiology, p.1117- 1121. 1989.
TAIZ, L.; ZEIGER, E. Fisiologia Vegetal. 3. ed. Porto Alegre: Artmed, 719p., 2013.
WOLF S, DEOM C. M., BEACHY R, LUCAS, W. J. Plasmodesmatal function is probed using transgenic tobacco plants that express a virus movement protein. Plant Cell. p. 593-604. 1991
NOLTE KD, KOCH KE. Companion-cell specific localization of sucrose synthase in zones of phloem loading and unloading. Plant Physiol. p. 899-905.1993.
HUMPHREYS T. E. A model for sucrose transport in maize scutellum. Phytochemishy. 679-684. 1978.
WINTER H., HUBER S.C. Regulation of sucrose metabolism in higher plants: localization and regulation of activity of key enzymes. Critical Reviews in Plant Science,p. 31- 67. 2000.
PATRICK J.W. Phloem unloading: Sieve element unloading and post-sieve element transport. Annual Review of Plant Physiology and Plant Molecular Biology. p. 165–190. 1997.
FROMMER, W. B., SONNEWALD, U. Molecular analysis of carbon partition in solanaceous species. Journal of Experimental Botany. p.587-607, 1995.
CUNHA, R. L. Tese: Crescimento, metabolismo do carbono e partição de assimilados, em resposta à manipulação da razão fonte/dreno, em Coffea Arabica L. sob condição de campo. 2007.