A equação de oxidação da água (ou foto-oxidação), descrita abaixo, indica que quatro elétrons são removidos de duas moléculas de água, gerando uma molécula de oxigênio e quatro íons de hidrogênio:![]()
A água é uma molécula muito estável; sua oxidação, e posterior formação de oxigênio molecular, é a fonte de quase todo o oxigênio na atmosfera terrestre.
Os prótons produzidos pela oxidação da água são liberados dentro do lume do tilacóide e não diretamente no compartimento estromal, devido a natureza vetorial da membrana e ao fato de o complexo produtor de oxigênio estar localizado na superfície interna do tilacóide. Esses prótons são, por fim, transferidos do lume para o estroma por translocação pela ATP sintase. Assim, os prótons liberados durante a oxidação da água contribuem para o potencial eletroquímico que irá operar na formação do ATP.
O manganês (Mn) é um cofator essencial no processo de oxidação da água e uma hipótese clássica postula que íons Mn sofrem uma série de oxidações – conhecidas como estados S e rotuladas S0, S1, S2, S3, S4 – possivelmente ligadas à oxidação da água e à geração de O2. Experimentos analíticos indicam que quatro íons Mn estão associados com cada complexo de liberação de oxigênio. Íons Cl– e Ca2+ são essenciais para a liberação do O2.
Um transportador de elétrons, geralmente identificado comoYz, funciona centre o complexo de liberação de oxigênio e o P680. Para funcionar nessa região, Yz necessita de uma forte tendência para reter os seus elétrons. Esta espécie foi identificada como um radical formado de um resíduo de tirosina na proteína D1 do centro de reação do PSII.
Após a excitação do PSII, há geração de um oxidante forte, que retorna seu estado de neutralidade a partir da extração de elétrons da água. A fotólise da água é catalisada pelo complexo de evolução da água, havendo transferência de quatro elétrons. Os prótons liberados no lúmen dos tilacóides contribuem para a geração de um gradiente de prótons para que possa haver geração de ATP.
O modelo do estado S postula um mecanismo de acúmulo de carga da luz através de cinco sucessivos estados de aumento de oxidação (S0 –> S4), no qual o S4 possui uma forte capacidade de oxidar a água (Figura 1). Vale ressaltar também que o único estado em que o S4 se encontra envolvido é o S4. Cada separação de cargas do P680/P680+ gera um acúmulo de carga de modo a avançar o estado de oxidação S. Além disso, cada ciclo requer quatro flashes de luz, ou seja, quatro fótons.
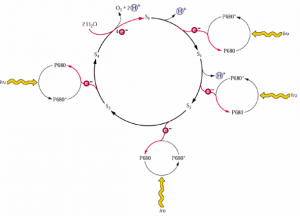
Figura 1. Modelo do complexo de evolução do oxigênio para fotólise da água
Cada fóton remove um elétron do P680, o qual é imediantamente resposto por um elétron extraído do aglomerado de manganês (S). A perda de um elétron do centro de manganês faz com que ele saia do S0 para o S4, oxidando a água e recuperando o estado S0.
